
論美國關稅及專利連結制度對我國學名藥之影響
文:張晏恂(思為國際專利商標事務所專利部副理/專利師)
一、引言
「從 2025 年 10 月 1 日開始,我們將對任何品牌或專利藥品徵收 100% 的關稅,除非這家公司正在美國建造藥品製造廠」美國總統川普在9月下旬一則Truth Social貼文裡寫道,為美國藥品市場與全世界的合作夥伴投下一枚震撼彈,此舉直接地衝擊海外製造品牌藥/專利藥輸往美國的藥品製造商,產業布局板塊隨之震動。
此前,衛生福利部表示,此項關稅政策主要針對品牌藥/專利藥,也就是所謂「原廠藥(original drug)」及「新藥(new medicine)」;目前普遍的認知中,此項關稅計畫並未涵蓋「原料藥(Active Pharmaceutical Ingredient, API)」及「學名藥(generic drug)」,而原料藥及學名藥構成臺灣出口到美國的大部分藥品;因此,由於原料藥/學名藥不在關稅計畫所及的範圍內,加上臺灣出口到美國的專利藥物相對稀少,對於國內藥廠的衝擊有限。
實際上,雖然此項關稅政策已暫緩實施,其所產生的不確定性對於國內藥廠產能布局的衝擊已然發酵。
無獨有偶,除了關稅變局,上路屆滿6年的「專利連結制度」也為國內藥品市場的專利戰爭添加新柴火,學名藥逐漸被排除在市場主流之外,而持續創高的健保藥費則幾乎全用在原廠藥上;無疑地,國內專利藥廠或學名藥廠的產能布局面臨國內外局勢的雙重挑戰,身處嚴峻且多變的局勢中,國內藥廠又是如何變換步伐、狹縫求存的呢?
二、因應美國關稅政策的國內藥品產能重置
白宮在10月1日即暫緩了進口品牌藥或專利藥加徵100%關稅的政策;然而,在這關稅海嘯第一排的國際大廠,包括羅氏(Roche)、諾華(Novartis)、阿斯特捷利康(AstraZeneca)、葛蘭素史克(GSK)、瑞士商艾伯維(AbbVie)、嬌生(Johnson & Johnson)、輝瑞(Pfizer)等品牌藥商,由於在美大量銷售專利藥,加上多數產品的產能布局分散於歐洲、亞太地區,迄今已相繼宣示或傳出加碼美國投資,以因應關稅與政府壓力。
相較於上述海外的品牌藥商,以製造原料藥及學名藥為導向,在臺設廠的品牌藥廠或本土藥廠,例如美時、永日、臺耀等,原則上不在100%關稅範圍,直接衝擊小。
然而,以CDMO (Contract Development and Manufacturing Organization,委託開發暨製造服務)1、CMO (Contract Manufacture Organization,委外生產服務)2導向、甚或擁有自主品牌藥的國內藥廠可就沒那麼幸運。
CDMO/CMO導向的藥廠由原廠授權製造品牌藥、專利藥或關鍵劑型,並輸出供應美國市場,這完全落入「美國以外的國家/地區設廠生產品牌藥或專利藥」的範圍;可以預期地,若維持美國境外的產能布局,將無可避免地被課予100%的藥品進口關稅;對此,品牌藥或專利藥訂單勢必將轉向美國本地。
下表1A羅列國內加入CDMO/CMO製造行列的多家藥廠及對應的產品與品牌藥廠,包括健喬信元、神隆(腫瘤類小分子藥物 API)、保瑞(口服固體、液劑、半固體、無菌注射)、臺灣東洋(脂質體)或永昕生物醫藥(細胞株/蛋白/單株抗體)等,以及下表1B則羅列擁有自主品牌藥的藥華藥(生物藥)、臺康生技(生物相似藥)或北極星藥業(抗癌新藥)等。
表1A
|
CDMO/CMO藥廠 |
劑型或製程 |
對應品牌藥廠 |
|
健喬信元 Synmosa |
鼻噴劑、發泡製劑、定量噴霧吸入劑、性荷爾蒙、顆粒劑 |
Boehringer Ingelheim、Kyowa Kirin、Kissei、Otsuka、Takeda |
|
神隆 ScinoPharm |
腫瘤類小分子 API |
Pfizer(Pfizer CentreSource / Pfizer CentreOne) |
|
保瑞 Bora(集團) |
無菌注射(小量至商業化)、口固劑、液劑、半固體 |
Accord BioPharma, Inc. |
|
臺灣東洋 TTY Biopharm |
脂質體、微球關鍵劑型 |
未具名(官方對外以「國際合作夥伴」稱之) |
|
永昕生物醫藥 MYCENAX |
細胞株/蛋白/單株抗體 |
未具名(官方對外以「國際合作夥伴」稱之) |
上述藥廠,在關稅變局發生實質衝擊前,已迅速地作出反應;保瑞在去年收購美國USL藥廠與Emergent BioSolutions無菌針劑廠,建立涵蓋口服、針劑、大分子藥物的完整產能,是眾家藥廠中率先落地美國投產者;藥華藥也在美國自建充填廠,新藥是實質在美國出廠;除美國投產避稅,積極拓展非美市場或在美尋求合作代工也是折衷的產能布局策略,例如神隆在2025年下半季積極拓展歐洲、南美及中東地區等地客戶,分散布局以降低關稅及政策不確定性的風險。
表1B
|
自主品牌藥廠 |
品牌藥品 |
境外授權藥廠 |
|
藥華藥 PharmaEssentia |
生物藥製劑 (長效干擾素) |
Pint-Pharma GmbH FORUS Therapeutics Inc. |
|
臺康生技 EirGenix |
生物相似藥 (凍晶注射劑) |
Sandoz AG |
|
北極星藥業 Polaris Group |
抗癌新藥 |
Tabuk Pharmaceutical Manufacturing Company、Er‑Kim Pharmaceuticals |
三、專利連結制度下的學名藥廠困境
「專利連結制度」的制度設計初衷在於,由食藥署管理專利登載平臺,便於學名藥廠在申請藥品許可時,比對新藥專利,以加速釐清學名藥有無侵犯新藥專利權,其具體制度架構如圖1所示。
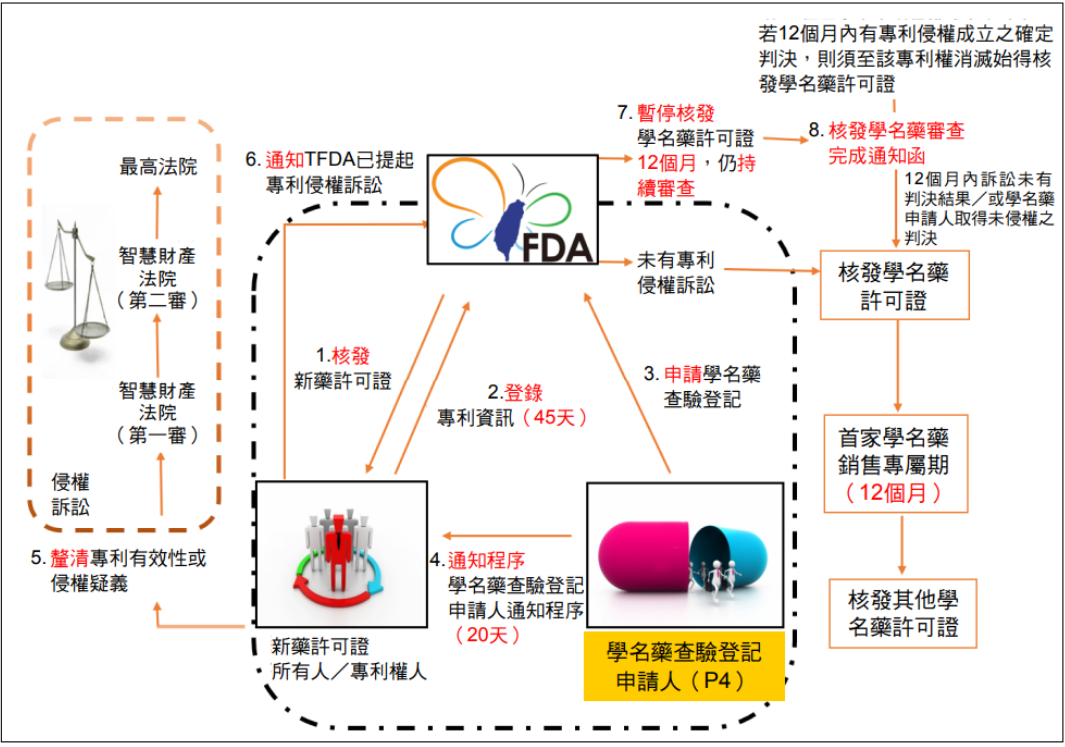
圖1. 專利連結制度的運作簡圖3
在專利連結制度上路後,食藥署核發新藥藥品許可證後,新證所有人須於期限內登載新藥專利資訊,而學名藥在藥證查驗登記階段,必須由以下四種情況擇一做出聲明:P1「無專利資訊」、P2「新藥專利權已消滅」、P3「學名藥同意在專利權消滅後再核發許可」、以及P4「主張未侵害新藥專利權、或新藥專利權應被撤銷」。
專利連結制度原本是為了減少學名藥上市後發生專利侵權訴訟,並使學名藥廠透過專利登載平臺確認是否侵害新藥專利權,期望為學名藥與專利藥之間創造出緩衝地帶,並鼓勵學名藥廠投入新藥開發或專利迴避設計。
一般而言,提出P1到P3聲明不生爭議,但提出P4聲明則是實質「挑戰」既存的專利權;在提出P4申請後,學名藥廠須主動通知新藥專利權人,以釐清學名藥是否侵害新藥專利權;然而,這無異於是給新藥專利權人一道開啟侵權訴訟的大門。
時至今日,由於專利連結制度導致的爭訟案件累積達到80餘件,已公開的訴訟裁判結果也累計達26件;除此之外,若兩造陷入侵權訴訟,還會導致學名藥許可證暫停核發12個月;縱然12個月內訴訟未有判決結果或學名藥廠取得未侵權之判決,可獲准學名藥藥品許可證,但已造成學名藥上市期程延宕。
此外,在藥證暫停核發期間,食藥署仍不中斷審查程序,學名藥廠也能申請健保核價,而若12個月內未被法院裁定侵權,也能在暫停核發期滿後取得藥證;話雖如此,此時學名藥廠不僅可能與新藥專利權人深陷纏訟,高機率進入二審、三審,也間接地影響醫療機構的採購意願;實質上,專利連結制度無可避免地加重學名藥廠的時間損失,大幅提高開發成本,還排擠原有的產能。
四、小結
因應美國總統川普上任後的關稅政策,多家國內藥廠赴美併購、或落地建廠投產;同時,部份廠商選擇開拓美國以外的廣大市場,使產能與市場布局更加靈活;然而,伴隨專利連結制度實施日久,原廠與學名藥廠的專利戰爭也日益激烈,不僅侵蝕國內學名藥市場份額,也削弱出口量能。
就在美國當地時間30日,參議院以51票贊同、47票反對的結果通過決議,要終止川普在全球範圍內實施的全面關稅政策,在短期內或可留給國內藥廠喘息的空間;僅短短一個月,政策風向峰迴路轉;或許,處在這巨大的不確定性中,政府應採取更為彈性的策略,嘗試放寬訴訟期間的學名藥出口豁免機制,同時鼓勵CDMO/CMO導向藥廠跨境合作生產,並強化自主品牌藥廠海外授權的媒合,以臺灣為研發中心投射至歐美、亞太地區投產,打造新一座護國神山。
**
註釋1:委託開發暨製造服務( Contract Development and Manufacturing Organization)是受藥證持有者(MAH)的委託進行各種醫藥品的外包生產服務,包括藥物、疫苗到醫材全都涵蓋在內,藉此,MAH可以委外、外包的方式來降低生產成本、加快產品上市腳步,接受CDMO委託的製造商則可以節省下藥物開發、臨床試驗到藥證審查的成本。
註釋2:委外生產服務(Contract Manufacture Organization)主要是接受生技/製藥公司的委託,提供生技產品生產時所需要的製程、配方開發、臨床試驗用藥、化學或生物合成的原料藥生產、中間體製造、製劑生產(如錠劑、針劑)以及包裝等服務。
註釋3:參考資料: 吳秀梅,淺談臺灣西藥專利連結制度,專利師,2019 年7 月,第39 期,頁2。

